Ý chính
2.1. Vật chất bao gồm các nguyên tố hóa học tinh khiết hoặc hỗn hợp; các nguyên tố kết hợp tạo thành hợp chất
2.2. Tính chất của một nguyên tố được xác định bởi cấu trúc nguyên tử của nó
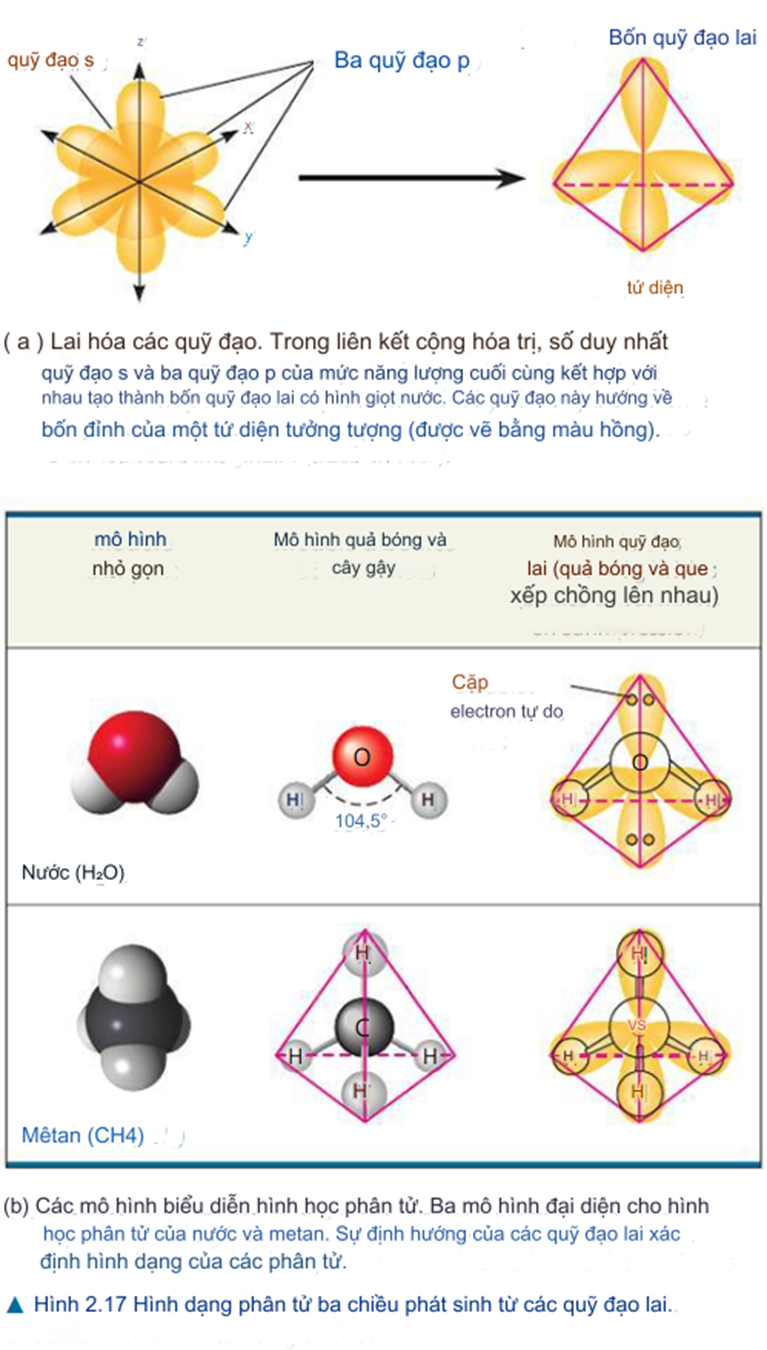
2.3. Sự hình thành và chức năng của phân tử phụ thuộc vào liên kết hóa học giữa các nguyên tử
2.4. Phản ứng hóa học tạo và phá vỡ liên kết hóa học
Giới thiệu



























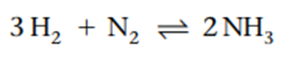

Opmerkingen